on UvA website: hims.uva.nl (Dutch: hims.uva.nl)
Researchers at the Universities of Amsterdam and Leiden together with the Netherlands Cancer Institute (Amsterdam) and Oncode Institute (Utrecht) have received a €10.6 million ERC Synergy Grant to develop innovative therapeutic approaches to target glioblastoma, a deadly primary brain tumour for which no curing therapy is yet available. At the heart of the proposed method are enzyme-mimicking molecular catalysts capable of producing various types of anti-cancer drugs within the tumour tissue itself. According to Joost Reek, professor of Supramolecular Catalysis at the University of Amsterdam (UvA) and coordinator of the ‘Cat4CanCenter’ research, this new approach could potentially solve many of the difficulties associated with the current treatment of glioblastoma.
Every year in the Netherlands some 500 to 700 people are diagnosed with glioblastoma. Neither surgery, radiotherapy, nor chemotherapy have yet provided a cure for this form of brain cancer. The challenge faced by surgical and radiotherapy teams is that the tumours are not sharply defined and invade deep into the surrounding brain tissue. The challenge for drug-based therapy is that glioblastoma cells are very effective in developing resistance. Even novel immunotherapy approaches – which have proved impressively successful in other solid tumours – have failed in the case of glioblastoma. This is largely due to a highly suppressive tumour microenvironment, where the so-called tumour-associated macrophages effectively ‘hijack’ the local immune response.
A radically new approach to chemotherapy
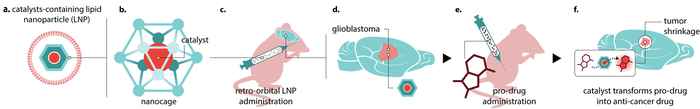
The advantage of this approach is that the tumour can be ‘loaded’ with high levels of drugs without the adverse effects normally associated with drug treatments. Current therapies involve administering high doses in the bloodstream to ensure that enough drugs can cross the blood-brain barrier and arrive at the brain tumour site. However, typically the resulting active dose in the tumour is relatively low, while the high dose in the blood results in concurrent toxicity and off-target side effects. By using non-toxic compounds, the new approach avoids these often severe complications.
Targeted delivery using lipid nanoparticles
Of course, the novel Cat4CanCenter approach also requires the components to cross the blood-brain barrier and to hit specific cell types in the tumour. For the pro-drugs this can be achieved through a dedicated molecular design. For the catalyst, this is ensured by using lipid nanoparticles that can carry compounds from the blood to the brain.
This is the expertise of Prof. Kros. “The brain is protected from foreign (bio)chemicals by the blood-brain barrier,” he explains. “It has shown to be a formidable barrier, rendering state-of-the-art drug delivery approaches that are successful in other therapies ineffective. In Cat4CanCenter we therefore develop radical new approaches to bring the catalysts inside the tumour by hijacking as yet unexplored existing biological pathways that are already present in the human body.”
Effective metal catalysis
“They now function in an aqueous environment, in the presence of biological molecules and even in living cells. By designing the cage so that is has affinity for the prodrug, we can make the catalyst operate in an enzyme-like fashion, boosting the conversion efficiency at low concentrations.”
He now hopes to unleash this power of metal catalysis for the treatment of cancer, but knows it will be challenging: “We need to make sure we can synthesise a whole range of drug molecules to combat all aspects of glioblastoma rapid growth.”

Concurrent remedies
on UvA website: hims.uva.nl (Dutch: hims.uva.nl)
Onderzoekers van de universiteiten van Amsterdam en Leiden hebben samen met het Nederlands Kanker Instituut (Amsterdam) en Oncode Institute (Utrecht) een ERC Synergy Grant van 10,6 miljoen euro ontvangen. Daarmee willen ze een nieuwe aanpak ontwikkelen voor de bestrijding van glioblastoom, een dodelijke primaire hersentumor waarvoor genezing nog niet mogelijk is. Centraal staan enzym-achtige moleculaire katalysatoren die in het tumorweefsel zelf kankermedicijnen produceren. Volgens prof. dr. Joost Reek, hoogleraar Supramoleculaire Katalyse aan de Universiteit van Amsterdam (UvA) en coördinator van het ‘Cat4CanCenter’, kan de nieuwe benadering veel problemen oplossen die een effectieve behandeling van glioblastoom nu nog verhinderen.

Elk jaar krijgen in Nederland zo’n 500 tot 700 mensen de diagnose glioblastoom. Voor deze vorm van hersenkanker is nog geen genezende behandeling beschikbaar. Chirurgie en radiotherapie kennen het probleem dat de tumoren niet scherp begrensd zijn en diep in het omringende hersenweefsel binnendringen. Behandeling met medicijnen is niet succesvol omdat glioblastoomcellen zeer effectief zijn in het ontwikkelen van resistentie. Zelfs nieuwe immuuntherapie, die al indrukwekkende resultaten opleverde bij andere typen tumoren, faalt in het geval van glioblastomen. Dit is grotendeels te wijten aan ‘tumorgeassocieerde macrofagen’ die de lokale immuunrespons effectief ‘kapen’.
Een radicaal nieuwe benadering van chemotherapie

Het voordeel van deze aanpak is dat de tumor wordt bestreden met hoge concentraties medicijnen zonder de nadelige effecten die daar normaal gesproken mee gepaard gaan. De huidige behandeling vereist hoge dosering in de bloedbaan om ervoor te zorgen dat genoeg medicijn de bloed-hersenbarrière kan passeren en de hersentumor bereiken. Doorgaans resulteert dit in relatief lage medicijnconcentraties in de tumor, terwijl de hoge dosis in het bloed tot ernstige bijwerkingen leidt. De nieuwe aanpak vermijdt deze complicaties vanwege het gebruik van niet-giftige pro-drugs.
Gerichte toediening met lipide nanodeeltjes

Effectieve metaalkatalyse
“Ze functioneren nu in een waterige omgeving, in aanwezigheid van biologische moleculen en zelfs in levende cellen. Als we de kooi zo ontwerpen dat er een zekere affiniteit is voor de prodrug, dan werkt de katalysator op een enzymachtige manier. Daardoor is ook bij lage concentraties een hoge omzettingsefficiëntie te realiseren.”
Hij hoopt nu deze potentie van metaalkatalyse te kunnen toepassen voor de behandeling van kanker, maar beseft dat de uitdaging groot is: “We moeten in staat zijn een hele reeks medicijnmoleculen te synthetiseren om alle aspecten van de snelle groei van glioblastoom te bestrijden.”